Наличие двух функциональных групп — аминогруппы –NH2 и карбоксильной группы –COOH — обеспечивает химические свойства аминокислот как у класса аминов и карбоновых кислот совместно.
Как и карбоновые кислоты, аминокислоты взаимодействуют со щелочами с образованием солей (Р.16.20):
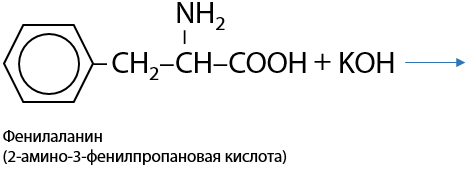

Образуются сложные эфиры (Р.16.21):
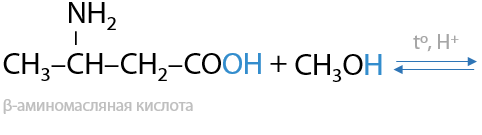
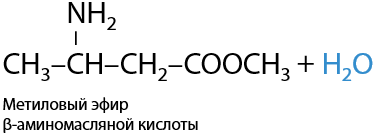
У сложных эфиров аминокислот невозможно образование ионов с двумя противоположно заряженными центрами. Такие соединения плохо растворяются в воде, но хорошо растворяются в органических веществах и их смесях: бензин, керосин, бензол C6H6, гексан C6H14.
Как и карбоновые кислоты, аминокислоты способны к декарбоксилированию в щелочной среде (Е.16.22):

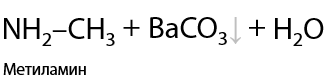
Аминогруппа проявляет основные свойства за счет наличия неподеленной электронной пары на атоме азота и может присоединять протон. В результате реакции образуется соль (Е.16.23):

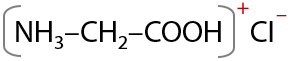
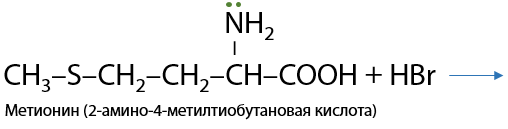

Как и первичные амины, аминокислоты реагируют с азотистой кислотой с выделением бесцветного газа N2 (Е.16.24), а аминогруппа замещается на гидроксигруппу –ОН (см. конспект «Амины»):


По количеству (объему) выделенного азота можно определить количество аминокислоты в анализируемом растворе (метод Ван-Слайка).
Важнейшее свойство аминокислот — образование пептидов. Пептиды — вещества, состоящие из нескольких остатков аминокислот, соединенных пептидной (амидной) связью (Е.16.25):
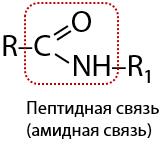
Пептиды образуются при взаимодействии нескольких аминокислот друг с другом: карбоксильная группа –COOH одной молекулы может взаимодействовать с –NH2 группой второй молекулы с отщеплением молекулы воды и т. д. (Е.16.26):


Заметим, что в структуре полученного дипептида (состоит из двух остатков аминокислот) остаются и аминогруппа, и карбоксильная группа, а значит реакция может продолжиться по любому из этих двух концов.
Образующиеся олигопептиды (состоят из 10-50 остатков аминокислот) или полипептиды (состоят из более чем 50 остатков аминокислот) из-за громоздкости формул записывают с применением трехбуквенных обозначений остатков аминокислот.
Например, следующая аминокислотная последовательность входит в состав одного из лекарственных препаратов, который применяется для лечения инсультов, язвы желудка, болезней зрительного нерва, для укрепления иммунной системы и повышения мозговой активности (16.27):

Аминокислоты содержат в своем составе атомы углерода, водорода, кислорода и азота, а значит будут сгорать с образованием углекислого газа CO2, воды Н2О и азота N2 (16.28):


Горение серосодержащих аминокислот и веществ других классов приводит к появлению еще одного продукта — сернистого газа SO2 (16.29):
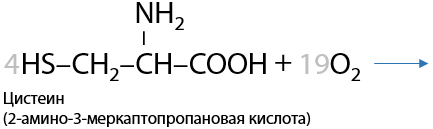
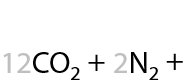
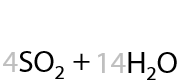
Ксантопротеиновая проба, от греч. «ксантос» — желтый. При нитровании аминокислот, содержащих в составе молекулы бензольное кольцо, образуются нитропроизводные желтого цвета (Е.16.30):
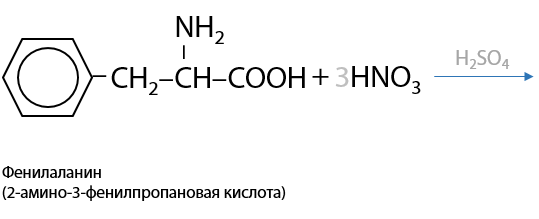

При написании продукта данной реакции помните о заместителях I и II рода. Необходимо учитывать, по каким положениям будет происходить замещение.
Реакция Фоля. При нагревании серосодержащих аминокислот, например, цистеина, в концентрированном растворе щелочи NaOH/KOH выделяется сульфид щелочного металла. Изменения цвета в реакции не происходит (Е.16.31):
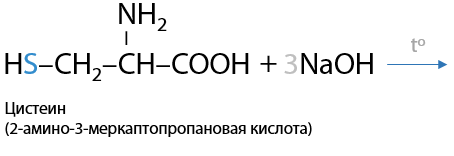
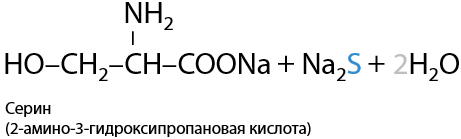
Обнаружение выделившегося сульфид-иона проводят с помощью солей свинца (II), которые в результате взаимодействия с ним образуют черный осадок PbS (Е.16.32):
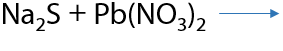

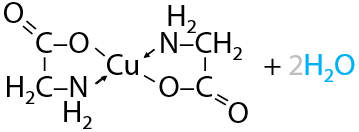
Подобно многоатомным спиртам аминокислоты способны образовывать комплексные соединения с катионами меди (II) синего цвета (Е.16.33):
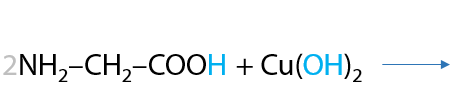
Все α-аминокислоты дают сине-фиолетовое окрашивание (пурпур Руэмана) в реакции с нингидрином за счет протекания окислительно-восстановительной реакции. В качестве побочного продукта выделяется углекислый газ СО2.
Вопрос по теме: