Бывает необратимой и обратимой (обратный процесс — ренатурация). Белки и пептиды под воздействием температуры, излучения или изменении кислотности среды (рН) могут изменять свое пространственное строение и терять характерные свойства. Разрушаются только водородные связи, первичная структура не изменяется (Е.17.12):
Классический и самый яркий пример денатурации — приготовление куриных яиц любым температурным методом (на сковороде или в микроволновой печи). Яичные белки прозрачные, жидкие и являются альбуминами, но при воздействии нагревания или микроволнового излучения теряют свои характерные свойства, становятся твердыми и белыми, а также перестают растворяться в воде.
Общее свойство для пептидов и белков. Разрушение белков и пептидов происходит под действием щелочей или кислот, а также специальных ферментов — протеаз, которые катализируют разрушение полипептидной цепи при воздействии воды. Гидролиз проходит до образования аминокислот или их солей. Ферментативный гидролиз можно характеризовать следующим уравнением (Е.17.13):
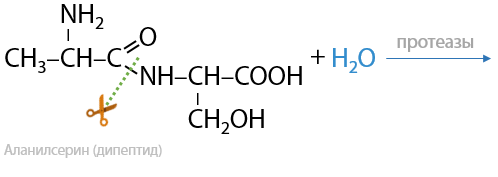
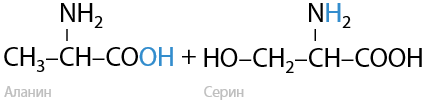
При использовании щелочей NaOH/KOH помимо гидролиза пептидов параллельно происходит образование солей из получившихся аминокислот. Реакция проходит по карбоксильной группе, побочным продуктом является вода (17.14):
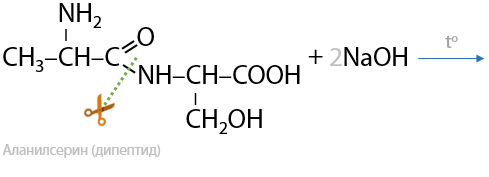

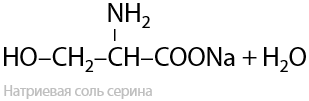
При использовании кислот помимо гидролиза пептидов тоже образуются соли, но реакция проходит уже по аминогруппе –NH2 (17.15):


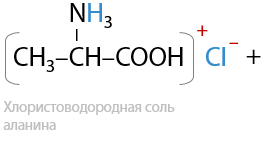
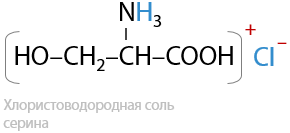
Заметьте, что при использовании неорганической кислоты в качестве гидролизующего агента воду необходимо дописывать в реагентах.
Как и другие органические вещества, содержащие азот, кислород и иногда серу, пептиды и белки сгорают до образования углекислого газа СО2, азота N2 и воды Н2О (присутствие серы обеспечивает образование еще и сернистого газа SO2).
Особенность сжигания пептидов и белков проявляется в характерном запахе «жженого рога» (из-за продуктов сгорания серы), который можно почувствовать, если сжечь пучок волос или шерстяную нитку.
Ароматические аминокислоты, входящие в состав полипептидной цепи, могут вступать в реакцию нитрования, как и индивидуальные аминокислоты (см. конспект «Аминокислоты). В результате реакции образуются нитропроизводные желтого цвета (Е.17.16):


Если в строении полипептидной цепи отсутствуют остатки ароматических аминокислот, т. е. включающих в состав бензольные кольца, то в результате ксантопротеиновой реакции не будет появления желтого окрашивания.
Биуретовая реакция. При взаимодействии растворов белков и пептидов, имеющих минимум две пептидные связи (–CO–NH–), с щелочным раствором солей меди (II) появляется фиолетовое окрашивание (17.17).
Вопрос по теме: