Анилин или фениламин — первый представитель класса ароматических аминов. Бесцветная маслянистая жидкость (при 25 °C), плохо растворяющаяся в воде (Р.15.43):

Наличие аминогруппы в строении обеспечивает особые свойства. Аминогруппа проявляет положительный мезомерный эффект (+М) и неподеленная электронная пара атома азота встраивается в общую электронную систему.
Именно по этой причине анилин и другие ароматические амины проявляют слабые основные свойства (Г.15.24):
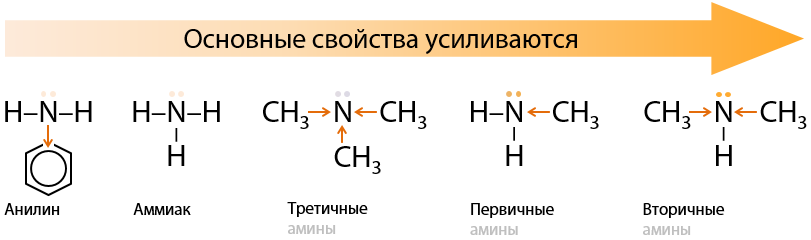
Из-за вовлечения неподеленной электронной пары атома азота в общую электронную систему бензольное кольцо «активируется» и реакции замещения проходят легче, чем у бензола. Такое же свойство наблюдалось и у фенола (см. «Химические свойства фенола»).
Аналогично восстановлению нитросоединений для получения неароматических аминов (Г.15.44):
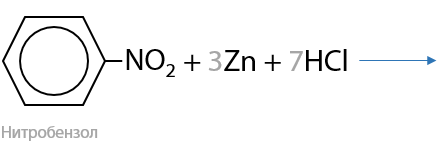
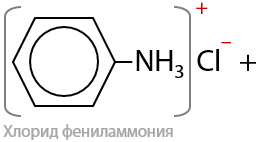
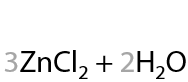
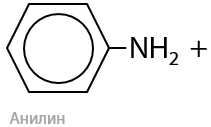
В оригинальном виде Н. Н. Зинин восстанавливал нитробензол с помощью сульфида аммония (Г.15.45):
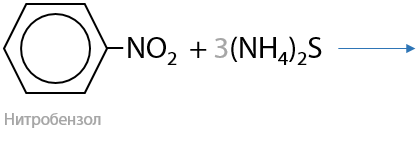
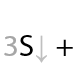

Не изменяет окраску индикаторов (так как не растворяется в воде, слабое основание).
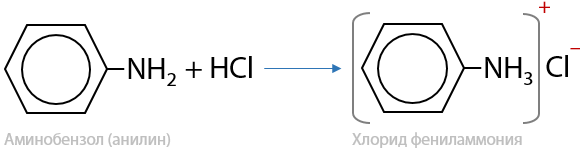
Из-за проявления слабых основных свойств анилин взаимодействует только с сильными неорганическими кислотами. Образуются соли фениламмония, в данном случае — хлорид фениламмония (Е.15.46):
Особое взаимодействие проявляется с азотистой кислотой HNO2. В данной реакции образуется соль фенилдиазония, которая в дальнейшем может использоваться для получения различных производных бензола (15.47):
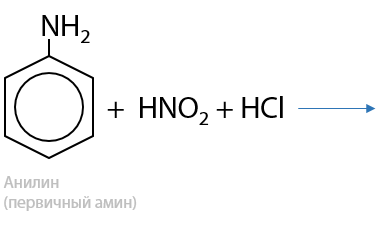

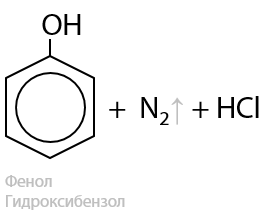
При нагревании в водной среде соли фенилдиазония гидролизуются и выделяется газообразный азот N2 (15.48):

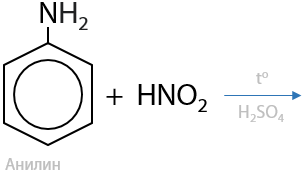
Таким образом, суммарная реакция анилина с азотистой кислотой на ЕГЭ следует записывать следующим образом (15.49):

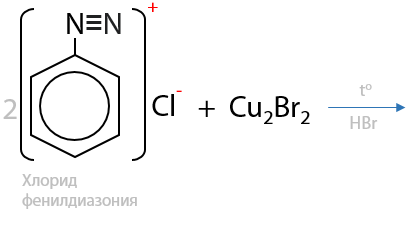
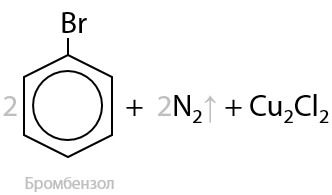
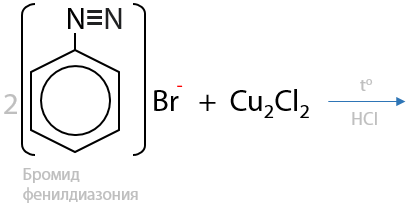
Соли фенилдиазония при взаимодействии с галогенидами меди (I) образуют арилгалогениды (15.50):
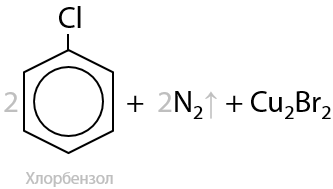
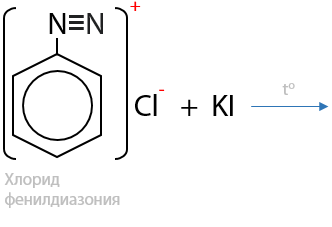
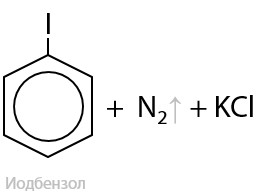
Взаимодействие соли фенилдиазония с иодидом калия образуется иодбензол (15.51):
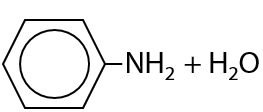
В результате гидролиза среда становится кислая и индикаторы меняют окраску, например, лакмус становится красный (15.52):


А гидроксид фениламмония в водной среде превращается в индивидуальный анилин, что приводит к помутнению раствора (анилин не растворяется в воде) (15.53):

Гидролиз солей фениламмония протекает быстрее в щелочной среде и раствор также становится мутным (15.54):

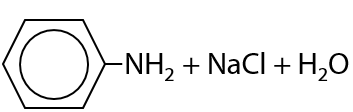
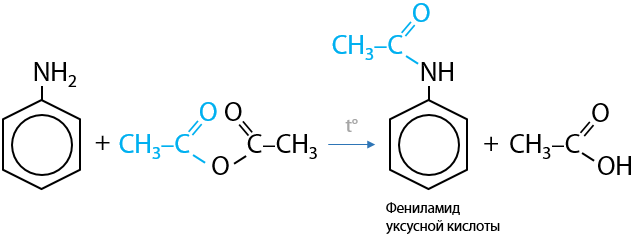
Анилин способен взаимодействовать с ангидридами карбоновых кислот, т. к. они являются хорошими ацилирующими агентами (см. «Функциональные производные карбоновых кислот») с образованием амидов (Г.15.55):
Качественная реакция. Происходит под действием бромной воды сразу в три положения без катализаторов. Реакция аналогична бромированию фенола (см. «Свойства фенола») (Г.15.56):
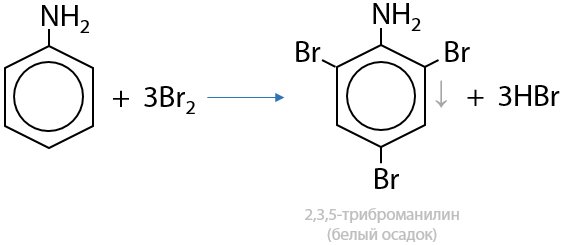
Важно. Признак реакции — белый осадок в виде хлопьев — также аналогичен признаку реакции при бромировании фенола, а значит отличить анилин от фенола бромной водой нельзя.
При смешивании нитрующей смеси азотной и серной концентрированных кислот в первую очередь происходит образование соли — нитрата фениламмония, и уже она вступает в процесс нитрования. Нитрование соли анилина может проходить по всем трем положениям (Е.15.57):

Чтобы соль не образовывалась и амино группа не протонировалась, ее следует защитить предварительной реакцией с галогенангидридом, а затем подвергать нитрованию (Е.15.58).
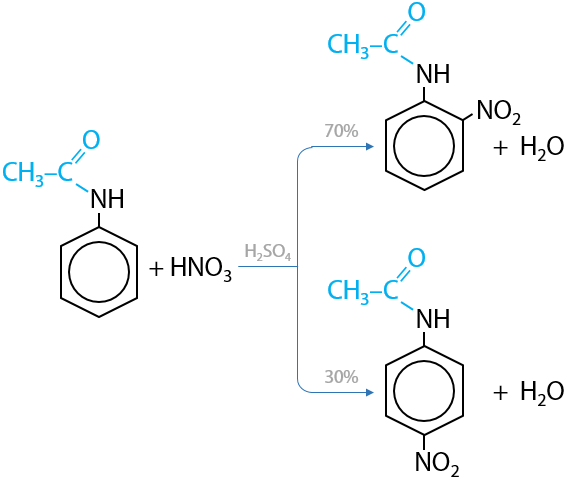
Таким образом, образуются только орто- и пара-замещенные нитропроизводные.
Вопрос по теме: