Правильный ответ
- Общая формула вещества CxHyBrz
n(CО2) = V : Vm = 7,62 : 22,4 = 0,34 моль
n(H2О) = m : M = 1,53 • 1 : 18 = 0,085 моль
n(H) = 2n(H2О) = 0,085 • 2 = 0,17 моль
m(HBr) = m(CxHyBrz) – m(C) – m(H) = 31,79 – 12 • 0,34 – 1 • 0,17 = 27,54 г
n(HBr) = m : M = 27,54 : 81 = 0,34 моль
nобщ.(H) = 0,17 + 0,34 = 0,51 моль
х : y : z = 0,34 : 0,51 : 0,34 = 1 : 1,5 : 1 = 2 : 3 : 2 = 4 : 6 : 4
Молекулярная формула: C4H6Br4
- Структурная формула
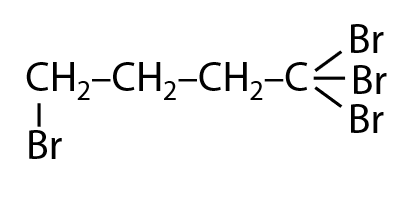
- Уравнение реакции
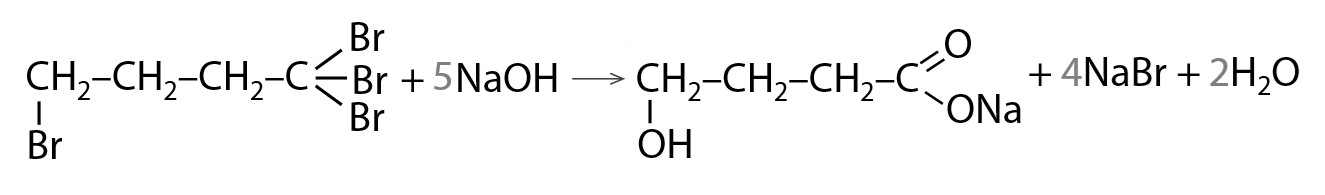
Максимальный балл: 3
Полное решение
- Общая формула вещества CxHyBrz
n(CО2) = V : Vm = 7,62 : 22,4 = 0,34 моль
n(H2О) = m : M = 1,53 • 1 : 18 = 0,085 моль
n(H) = 2n(H2О) = 0,085 • 2 = 0,17 моль
m(HBr) = m(CxHyBrz) – m(C) – m(H) = 31,79 – 12 • 0,34 – 1 • 0,17 = 27,54 г
n(HBr) = m : M = 27,54 : 81 = 0,34 моль
nобщ.(H) = 0,17 + 0,34 = 0,51 моль
х : y : z = 0,34 : 0,51 : 0,34 = 1 : 1,5 : 1 = 2 : 3 : 2 = 4 : 6 : 4
Молекулярная формула: C4H6Br4
- Структурная формула
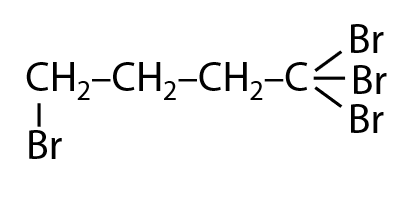
- Уравнение реакции

Максимальный балл: 3