Реакции присоединения
Из-за того, что в карбонильной группе происходит перераспределение электронной плотности π-связи и возникают частичные заряды на атомах углерода и кислорода соответственно, то взаимодействие кетонов и альдегидов с некоторыми другими веществами осуществляется посредством электростатического взаимодействия: «плюс притягивается к минусу, минус притягивается к плюсу» (Е.11.20):
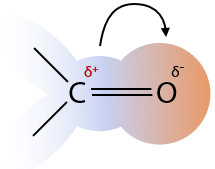
1) Присоединение водорода
Присоединение водорода происходит в присутствии металлических катализаторов, например никеля. В результате образуются вторичные спирты (Г.11.21):
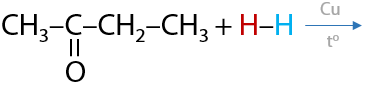
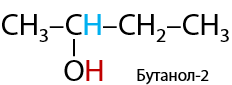
2) Присоединение циановодорода HCN
Как и у альдегидов, при присоединении циановодорода (синильной кислоты) по карбонильной группе образуются вещества, содержащие при одном атоме углерода гидроксильную группу –ОН и цианогруппу –CN. Такие вещества относятся к классу циангидринов (Е.11.22):
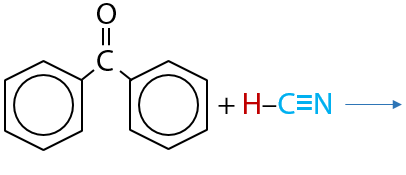

Единственное отличие от альдегидов, что гидроксильная группа и цианогруппа в результате реакции оказываются при вторичном атоме углерода, т. е. углеродная цепь в данном случае разветвляется (см. раздел «Химические свойства альдегидов»). В последствии реакцию используют для удлинения углеродной цепи на один атом углерода.
3) Присоединение гидросульфита натрия NaHSO3
Качественная реакция. Кетоны, как и альдегиды, при взаимодействии с гидросульфитом натрия образуют сульфопроизводные, которые выпадают в форме белого осадка из раствора (Е.11.23):
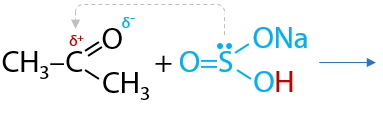
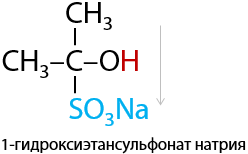
Полученные сульфопроизводные легко разлагаются в кислой среде с получением исходного кетона (Г.11.24):
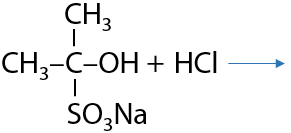
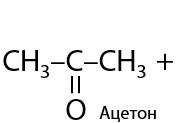
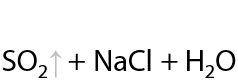
Ранее эти осадки использовали для идентифицирования альдегидов и кетонов, т. к. сульфопроизводное определенного альдегида имеет конкретную температуру плавления, зная которую можно точно установить структуру исходного карбонильного соединения.
4) Присоединение реактивов Гриньяра
Вещества, образуемые при взаимодействии магния с моногалогеналканами, были открыты Виктором Гриньяром и названы в его честь (Г.11.25):


В таких соединениях электронная плотность сильно смещена от атома магния к углероду, за счет чего связь C – Mg легко разрывается. Такое свойство реактивов Гриньяра способствует их присоединению по карбонильной группе кетонов (Г.11.26):
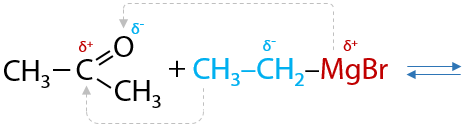
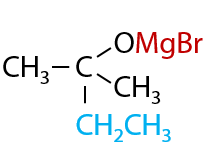
Магнийорганическое производное подвергается гидролизу в кислой среде, в результате чего из кетонов в две стадии образуются третичные спирты (Г.11.27):
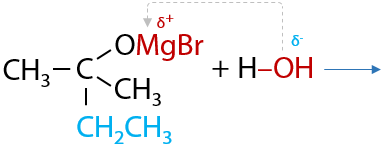
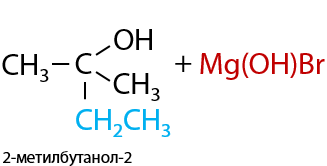
Присоединение реактива Гриньяра к альдегидам приводит к образованию вторичных спиртов, а к кетонам — к образованию третичных спиртов. Все зависит от количества углеводородных заместителей рядом с карбонильной группой в исходном соединении. (см. раздел «Химические свойства альдегидов»)
Реакции окисления
5) Горение
По сравнению с альдегидами, которые окисляются даже кислородом воздуха без нагревания, кетоны очень устойчивы к воздействию окислителей. В целом, интерес представляет только реакция полного окисления, т. е. горения (Г.11.28):
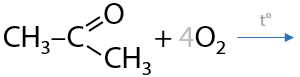

6) Окисление циклических кетонов
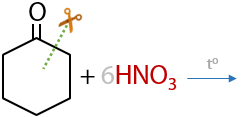
Циклические кетоны могут окисляться с раскрытием цикла концентрированной азотной кислотой HNO3 с получением дикарбоновых кислот (11.29):

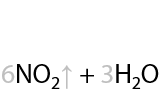
Реакции замещения
7) Замещение в углеводородном заместителе
Кетоны, как и альдегиды, могут взаимодействовать с хлором в щелочной среде. Замещение атома водорода на атом галогена при этом происходит при α-углеродном атоме, т. к. именно с него карбонильная группа стягивает большее количество электронной плотности, что облегчает протекание замещения (Г.11.30):
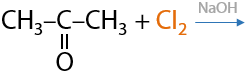
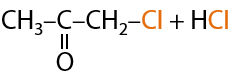
С бромом формально происходит аналогичная реакция, только реакция проводится между двумя растворами. Скорость реакции с бромом меньше, чем хлором, из-за его меньшей активности. Качественный признак такой реакции обесцвечивание раствора (Е.11.31):

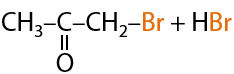
В результате бромирования образуются вещества со слезоточивым действием — лакриматоры, которые используются в баллончиках для самообороны.
При избытке галогена возможно замещение всех атомов водорода при α-углеродном атоме (Г.11.32). Такое встречается при взаимодействии ацетона со щелочным раствором иода. Качественный признак реакции: выпадение желтого осадка иодоформа CHI3, обладающего запахом «больницы».

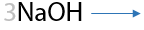
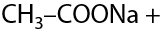
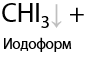
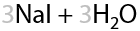
8) Замещение атома кислорода в карбонильной группе
При взаимодействии кетонов, как и альдегидов, с хлоридом фосфора (V) атом кислорода альдегидной группы замещается на два атома хлора (Е.11.33). Побочный продукт реакции — оксохлорид фосфора (V):


Отличие реакции от альдегидов в том, что образуются геминальные дигалогенпроизводные, в которых два атома галогена стоят при вторичном атоме углерода (см. раздел «Химические свойства альдегидов»).
Сложность реакции заключается в подборе растворителя для ее проведения. В водных или щелочных растворах дигалогенпроизводные подвержены гидролизу с образованием исходного кетона (см. раздел «Получение кетонов»)