Арены — циклические ароматические углеводороды, имеющие бензольный фрагмент в своем составе. Первый представитель аренов — бензол — он был выделен из нефти Майклом Фарадеем, но не был похож по свойствам на другие известные вещества. Поэтому только после открытия теории строения органических соединений была установлена его структура А. Кекуле (Е.6.1):
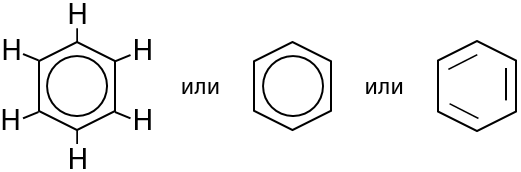
Все атомы углерода бензольного кольца находятся в sp2-гибридизации, σ-связи С–С и С–Н образуют плоский шестиугольник, а негибридные р-орбитали атомов углерода — единое π-электронное облако, которое является той самой ароматической системой.
На изображениях электронного строения σ- и π-связей в молекуле бензола заметьте, что у него не существует отдельных одинарных и двойных связей в структуре кольца. Электронная плотность p-орбиталей объединяется (Е.6.2):
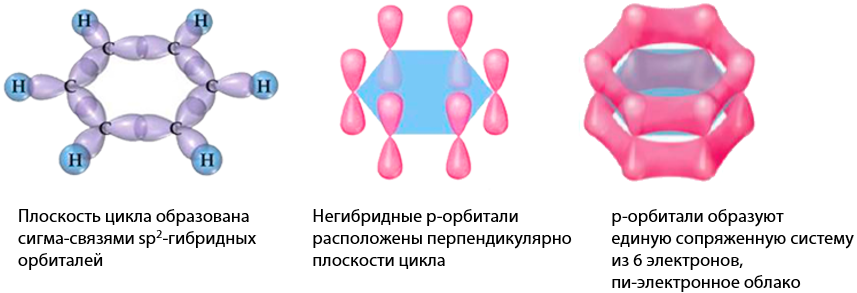
Ароматическая π-электронная система, состоящая из 6 электронов, обладает повышенной устойчивостью. Если сравнить гипотетический циклотриен и бензол, то примерный выигрыш в энергии бензола будет составлять 150 кДж/моль (энергия стабилизации).
Гомологи бензола
При замещении атомов водорода в молекуле бензола на алкильные (углеводородные) заместители будут получены гомологи бензола, отличающиеся от С6Н6 на N-е количество фрагментов –CH2–, т. е. гомологических разностей (Е.6.3):
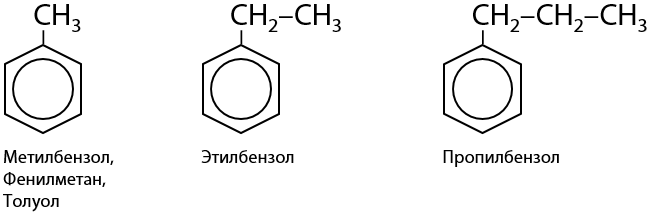
Гомологи бензола одновременно проявляют свойства и ароматических соединений за счет наличия ароматического кольца, и насыщенных углеводородов за счет наличия предельных алкильных заместителей. Если в структуре углеводородного заместителя находится ненасыщенный фрагмент (кратная связь), например, как у стирола, то проявляются также свойства и непредельных углеводородов (6.4).
