Правильный ответ
- Вычислим массовую долю NaOH в итоговом растворе.
m итог. p-pa = m(I2) + m(Zn) + m(NaOH) р-ра − m(Н2) = 33,02 + 13 + 200 − 0,14 = 245,88 г
ω (NaOH) = m в-ва : m p-pa • 100% = 13,6 : 245,88 • 100% = 5,53%
Полное решение
- Запишем уравнения реакций
(1) Zn + I2 = ZnI2
(2) Zn + 2NaOH + 2H2O= Na2[Zn(OH)4] + H2 ↑
(3) ZnI2 + 4NaOH = Na2[Zn(OH)4] + 2NaI
- Вычислим массу компонентов исходной смеси (Zn и I2).
n(H2) = V : Vm = 1,568 : 22,4 = 0,07 моль
n(I2) = х моль,
n1(Zn) = n(I2) = х моль (по уравнению 1)
n2(Zn) = n(H2) = 0,07 моль (по уравнению 2)
n(Zn) = n1(Zn) + n2(Zn) = х + 0,07
m(I2) = M • n = 254x
m(Zn) = M • n = 65(x + 0,07) = 65x + 4,55
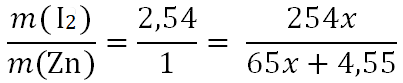
х = 0,13 моль
m(I2) = M • n = 254 • 0,13 = 33,02 г
m(Zn) = m(I2) : 2,54 = 33,02 : 2,54 = 13 г
- Вычислим массу остатка NaOH.
n(NaOH) = 2 • n(Zn) = 2 • 0,07 = 0,14 моль (по уравнению 2)
n(NaOH) = 4 • n(ZnI2) = 4 • 0,13 = 0,52 моль (по уравнению 3)
n(NaOH) прореаг. = 0,14 + 0,52 = 0,66 моль
m(NaOH) прореаг. = M • n = 40 • 0,66 = 26,4 г
m(NaOH) исх. = m p-pa • ω : 100% = 200 • 20 : 100 = 40 г
m(NaOH) ост. = m(NaOH) исх. − m(NaOH) прореаг. = 40 – 26,4 = 13,6 г
- Вычислим массовую долю остатка NaOH в итоговом растворе.
m(H2) = M • n = 2 • 0,07 = 0,14 г
m итог. p-pa = m(I2) + m(Zn) + m(NaOH) р-ра − m(Н2) = 33,02 + 13 + 200 − 0,14 = 245,88 г
ω (NaOH) = m в-ва : m p-pa • 100% = 13,6 : 245,88 • 100% = 5,53%