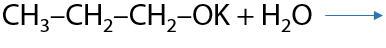Промышленные способы
1) Окисление метана
Процесс получения метанола CH3OH. Исторический, проблемный способ — невозможно остановить окисление на метаноле, оно продолжается до формальдегида H2C=O, муравьиной кислоты HCOOH или углекислого газа CO2 (Г.7.16):
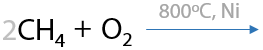

Параллельно происходящие процессы окисления (Е.7.17):
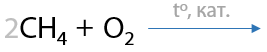

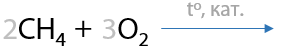

2) Метанол из синтез-газа
Лучший способ получения. Катализаторы: Cr2O3, ZnO (Г.7.18):
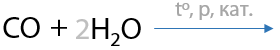

3) Гидратация этилена
Процесс получения этанола. Используют только для промышленных целей, дешевый способ. Полученный спирт — синтетический (Г.7.19):

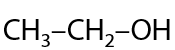
Гидратация алкенов является обратимой реакцией, т.к. дегидратация спиртов с образованием исходных алкена и воды происходит при этих же условиях.
4) Спиртовое брожение глюкозы
Процесс получения этанола для пищевой промышленности и медицины (Г.7.20):

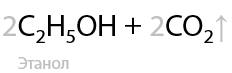
5) Восстановление карбонильных соединений
Сильные восстановители переводят карбонильную группу в спиртовую. Часто для такого превращения используют водород в присутствии металлических катализаторов (Г.7.21):
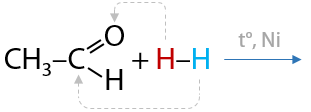

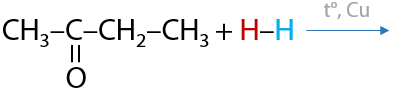
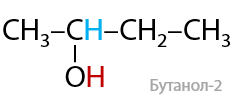
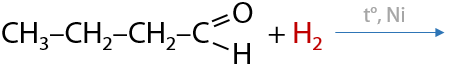
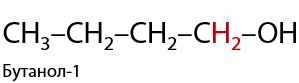
Первичные спирты получают восстановлением альдегидов.
Вторичные спирты получают восстановлением кетонов.
Лабораторные способы
6) Гидратация алкенов
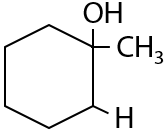
Реакция проходит по ионному механизму и является обратимой, катализируется кислотами — используют серную H2SO4 или ортофосфорную H3PO4 кислоты. Присоединение проходит по правилу Марковникова (Г.7.22):
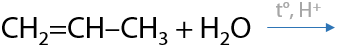

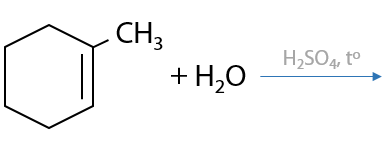
7) Гидролиз галогеналканов
Гидролиз галогеналканов проходит по ионному механизму только в водной среде и является необратимым процессом (Г.7.23):

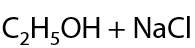
Конкурирующий процесс — отщепление галогеноводорода. Чтобы провести реакцию отщепления необходим спиртовой раствор щелочи (Г.7.24).
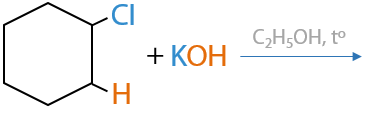

8) Гидролиз алкоголятов (реакция из ЕГЭ)
Алкоголяты способны разрушаться (гидролизоваться) в присутствии воды. Обратите внимание, что данный процесс является необратимым, т. к. спирты не реагируют со щелочами: