Правильный ответ
- Запишем уравнения реакций
(1) 2Ag + 2H2SO4 = Ag2SO4 + SO2↑ + 2H2O
(2) 2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑
- Определим массы металлов
Пусть V(SO2) = х л, V(H2) = y л. Тогда n(SO2) = х моль, V(H2) = y моль.
V(SO2) = 2V(H2) (по условию задачи)
n(SO2) = 2n(H2)
x = 2y
n(H2SO4)1 = 2n(SO2) = 2x (по уравнению реакции 1)
n(H2SO4)2 = n(H2) = у (по уравнению реакции 2)
m(H2SO4)общ = m(H2SO4)1 + m(H2SO4)2 = 98 · (2х + у) = 36,75 г
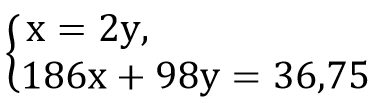
х = 0,15 моль; у = 0,075 моль
- Определим массу серебра и алюминия
n(Ag) = 2n(SO2) = 2 · 0,15 = 0,3 моль
m(Ag) = n · M = 0,3 · 108 = 32,4 г
n(Al) = 2 : 3 · n(H2) = 2 : 3 · 0,075 = 0,05 моль
m(Al) = n · M = 0,05 · 27 = 1,35 г
- Определим, во сколько раз масса алюминия меньше массы серебра
m(Аg) : m(Аl) = 32,4 : 1,35 = 24
Полное решение
- Запишем уравнения реакций
(1) 2Ag + 2H2SO4 = Ag2SO4 + SO2↑ + 2H2O
(2) 2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑
- Определим массы металлов
Пусть V(SO2) = х л, V(H2) = y л. Тогда n(SO2) = х моль, V(H2) = y моль.
V(SO2) = 2V(H2) (по условию задачи)
n(SO2) = 2n(H2)
x = 2y
n(H2SO4)1 = 2n(SO2) = 2x (по уравнению реакции 1)
n(H2SO4)2 = n(H2) = у (по уравнению реакции 2)
m(H2SO4)общ = m(H2SO4)1 + m(H2SO4)2 = 98 · (2х + у) = 36,75 г
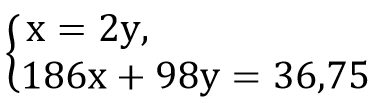
х = 0,15 моль; у = 0,075 моль
- Определим массу серебра и алюминия
n(Ag) = 2n(SO2) = 2 · 0,15 = 0,3 моль
m(Ag) = n · M = 0,3 · 108 = 32,4 г
n(Al) = 2 : 3 · n(H2) = 2 : 3 · 0,075 = 0,05 моль
m(Al) = n · M = 0,05 · 27 = 1,35 г
- Определим, во сколько раз масса алюминия меньше массы серебра
m(Аg) : m(Аl) = 32,4 : 1,35 = 24